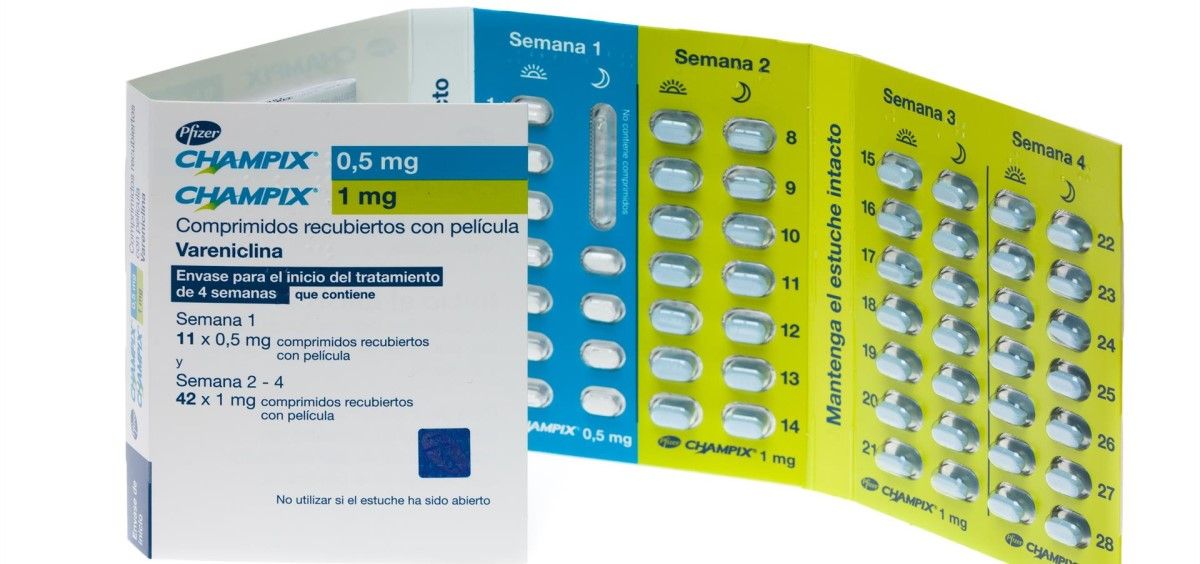
La Agencia Española de Medicamentos y Productos Sanitarios (Aemps) ha informado este martes de un problema de suministro del medicamento para dejar de fumar 'Champix', debido a que se ha parado su distribución mientras se investiga la detección de una impureza en el citado fármaco. Por este motivo, de manera preventiva, se han retirado del mercado tres lotes del mismo.
Ante esta situación la Aemps recomienda que no se inicien nuevos tratamientos ya que no se puede garantizar su continuidad, mientras que a los pacientes que ya estén en tratamiento y que no puedan completarlo por el problema de suministro, les recomienda que se dirijan a su médico para que valore el cambio a otro medicamento.
La Aemps informa de que el titular de autorización de comercialización de 'Champix' (vareniciclina), Pfizer Europe MA EEIG (Pfizer), ha parado la distribución de nuevas unidades debido a que se está investigando la presencia de la impureza N-nitrosovareniclina en el citado medicamento.
Por ello se ha ordenado la retirada de manera preventiva en almacenes mayoristas y oficinas de farmacia de tres lotes distribuidos en España para los cuales Pfizer ha solicitado su retirada voluntaria, debido a la detección de la citada impureza en niveles superiores al límite que ha establecido la compañía.
La compañía estima que previsiblemente en septiembre se haya restablecido el suministro
Se trata de los lotes 00019060 y 00020450 de 'Champix' 0,5 mg y 1 mg comprimidos recubiertos con película 11x 0,5 mg + 14 x 1 mg + 28 x 1 mg (NR: 106360023, CN: 697864), y el lote ED7396 de 'Champix' 0,5 mg comprimidos recubiertos con película, 56 comprimidos (NR: 06360001, CN: 656184).
Como consecuencia de ello, informa de que quedan unidades limitadas en los almacenes mayoristas y oficinas de farmacia de las cuatro presentaciones de 'Champix'. La compañía estima que previsiblemente en septiembre se haya restablecido el suministro.
El hallazgo de esta impureza es resultado de las nuevas medidas que se han adoptado en la Unión Europea para garantizar que las estrategias de control son adecuadas para prevenir o limitar la presencia de este tipo de impurezas tanto como sea posible, explica la Aemps.
Así, en medicamentos en los que se ha detectado previamente este tipo de impurezas, el riesgo ha sido bajo y las autoridades han establecido estrictos límites. La presencia de esta impureza está siendo evaluada por parte de la Agencia Europea del Medicamento (EMA, por sus siglas en inglés) y de las autoridades nacionales competentes de la Unión Europea para establecer las acciones regulatorias necesarias.